Last updated: 22 Aug 25 18:30:05 (Asia/Shanghai)
胸科、甲乳科疾病
This tutorial is powered by Bensz/黄伟斌
速记
考点速记清单
| 模块/疾病 | 高频考点 | 速记要点/口诀 |
|---|---|---|
| 甲状腺应用解剖 | 外侧喉上神经保护 | 上极血管结扎靠腺体侧,避免高位结扎致声调下降,“高音唱不上去”。 |
| 甲状腺应用解剖 | 喉返神经易损点 | 入喉点在环杓关节旁;Berry韧带处锐性分离,沿气管食管沟追踪神经。 |
| 甲状腺应用解剖 | 甲状旁腺与血供 | 多位于甲状腺后缘;主要供血来自下甲状腺动脉末支;必要时自体移植预防低钙。 |
| 甲状腺应用解剖 | 术中出血来源 | 峡部/下极下甲状腺静脉丛撕裂最常见;逐支结扎,术野清晰。 |
| 单纯性甲状腺肿 | 最常见病因 | 碘缺乏;TSH代偿升高→滤泡增生;放碘摄取弥漫增高。 |
| 单纯性甲状腺肿 | 治疗首选 | 补碘(碘盐/碘化钾);压迫/胸骨后/美容或疑恶变→手术。 |
| 甲亢外科 | 术前准备三件套 | 抗甲药+β阻滞+卢戈碘(术前10–14天);目标达甲功近正常。 |
| 甲亢外科 | 术式与并发症 | 近全/全切降复发;颈前血肿立即开口减压;低钙见Trousseau/Chvostek征。 |
| 亚急性甲状腺炎 | 诊断三联 | 颈前疼痛+ESR高+放碘摄取显著降低;抗体多阴性。 |
| 亚急性甲状腺炎 | 治疗要点 | NSAIDs或糖皮质激素;不需抗甲状腺药;低功能期短期左甲状腺素。 |
| 桥本甲状腺炎 | 抗体与超声 | 抗TPO/抗TG高滴度;超声弥漫低回声、“橡皮样”肿大,易转甲减。 |
| 桥本甲状腺炎 | 警示并发症 | 腺体快速增大警惕甲状腺淋巴瘤;治疗以左甲状腺素替代为主。 |
| 甲状腺癌 | 类型与转移 | 乳头状(最常见、淋巴转移);滤泡(血行骨/肺);髓样(降钙素↑、RET);未分化(进展快)。 |
| 甲状腺癌 | 手术与术后 | 低危≤1cm单灶可“腺叶+峡部”;中高危/多灶/放射史/髓样→全切±中央区清扫;分化型131I+TSH抑制。 |
| 甲旁腺亢进 | 最常见病因 | 原发性以单发腺瘤最多;实验室:Ca↑、P↓、PTH↑(原发)。定位首选MIBI。 |
| 甲旁腺亢进 | 治疗与鉴别 | 腺瘤切除;弥漫增生行3.5腺切除;鉴别FHH(尿钙低)。高钙危象先补液+袢利尿+双膦酸盐。 |
| 急性乳腺炎 | 病原与处理 | 哺乳2–6周,金黄色葡萄球菌多见;继续排空乳汁+抗菌;脓肿切开引流。 |
| 乳腺囊性增生 | 典型表现与诊断 | 周期性胀痛、双侧多发小结节;穿刺抽出清亮液体后肿块消退。 |
| 乳房纤维腺瘤 | 良性特征与处理 | 可推动、界清,年轻女性;>3cm/生长快/可疑影像→切除。 |
| 导管内乳头状瘤 | 单孔血性溢乳 | 多位于乳晕后;首选微乳管切除,病理评估是否伴不典型/癌变。 |
| 乳房肉瘤 | 治疗关键 | 广泛局部切除确保切缘;腋窝清扫不常规。 |
| 乳腺癌 | 综合治疗路径 | 早期可保乳+SLNB+放疗;ER/PR阳性→内分泌;HER2阳性→抗HER2;三阴性/高危→化疗;炎性乳腺癌新辅助化疗优先。 |
| 肋骨骨折 | 要点与并发 | 镇痛+呼吸锻炼;连枷胸机械通气;合并气/血胸→胸管。 |
| 气胸 | 张力性急救 | 临床诊断即刻针刺减压(优选第4–5肋间腋前/中线)→胸腔闭式引流。 |
| 血胸 | 大量血胸开胸指征 | 初次引流>1500 mL或持续>200 mL/h×2–4h,或血流动力学不稳;先粗胸管+复苏。 |
| 脓胸 | 胸液特征与处理 | 脓性、pH<7.2、糖低、LDH高;抗生素+充分引流;分隔用tPA/DNase;机化期VATS剥脱。 |
| 食管癌 | 核心诊断与分期 | 进行性吞咽困难;确诊靠内镜活检;内镜超声评估T分期;CT/PET-CT查转移。 |
| 食管癌 | 治疗分层 | T1a行EMR/ESD;可切除局限期:食管切除+系统清扫,新辅助放化疗提R0率;不宜手术:根治放化疗。 |
| 纵隔肿瘤 | 前纵隔4T | Thymoma胸腺瘤(合并重症肌无力)、Thyroid异位甲状腺、Teratoma畸胎瘤、Terrible lymphoma淋巴瘤。 |
| 纵隔肿瘤 | 后纵隔最常见 | 神经源性肿瘤;MRI评估椎管;手术切除效果佳。生殖细胞瘤查AFP/β-hCG。 |
高频易错点小册
| 知识点 | 易错说法 | 正确要点 | 记忆提示 |
|---|---|---|---|
| 甲亢术前准备 | 只用抗甲药即可手术 | 需抗甲药+β阻滞+卢戈碘,达甲功近正常再手术 | “抗β碘三步走” |
| 甲亢术后并发症 | 颈前血肿加压观察 | 立即拆线开口减压,防窒息 | “颈肿先开,不等检查” |
| 亚急性甲状腺炎 | 甲亢期应用抗甲状腺药 | 不需抗甲药;用NSAIDs/激素+β阻滞对症 | “破坏性甲亢不产新激素” |
| 桥本与Graves | 均为摄碘率升高 | 桥本多摄取正常/低;Graves弥漫增高 | “G高H(Hashimoto)低” |
| 甲状腺外侧喉上神经 | 上极血管应远离腺体高位结扎 | 上极血管靠腺体侧分离结扎以护神经 | “贴腺体保高音” |
| 甲状腺癌手术范围 | 所有乳头状癌均需全切 | 低危单灶≤1 cm可腺叶+峡部切除 | “微癌可保半边” |
| 分化型与髓样癌 | 术后随访都看甲状腺球蛋白 | 分化型看甲状腺球蛋白;髓样癌看降钙素/CEA | “髓样=钙素” |
| 髓样癌治疗 | 术后可用131I | 不摄碘,131I无效;需全切+中央区清扫 | “C细胞不吃碘” |
| 甲旁亢化验 | PTH高=继发性 | 原发:Ca↑、P↓、PTH↑;继发:Ca低/正、PTH↑ | “原高钙,继不高” |
| 甲旁亢定位 | 超声是首选 | MIBI显像为首选定位,超声为补充 | “找旁腺,先MIBI” |
| 甲旁增生术式 | 增生做全切 | 行3.5腺切除或全切+自体移植 | “留半腺,保生理” |
| 急性乳腺炎 | 需停止哺乳 | 继续排空乳汁;脓肿切开引流 | “通则不痛,空则不脓” |
| 囊性增生与癌 | 疼痛更像癌 | 囊性增生周期性胀痛常见;癌多无痛质硬 | “痛多良,硬多恶” |
| 导管内乳头状瘤 | 多孔溢乳也可考虑乳头状瘤 | 典型为单孔血性溢乳;多孔需警惕恶性 | “一孔血=乳头瘤” |
| 乳房肉瘤 | 常规行腋窝清扫 | 淋巴转移少,不常规清扫;重在足够切缘 | “肉瘤靠切缘” |
| 保乳指征 | 早期即可保乳,无需放疗 | 保乳后必须放疗以降局部复发 | “保乳必放” |
| 张力性气胸 | 先拍片确认再处理 | 临床诊断即先针刺减压后胸管 | “先针后管,不等片子” |
| 胸管置入部位 | 第2肋间锁骨中线最佳 | 首选第4–5肋间腋前/中线;第2肋间穿透失败率高 | “腋中四五更安全” |
| 大量血胸阈值 | 持续出血>100 mL/h即开胸 | 标准为>200 mL/h×2–4h或初次>1500 mL | “1500起步,200持续” |
| 脓胸判定指标 | 看蛋白/LDH即可 | 关键是胸液pH<7.2或糖低+细菌阳性;LDH高为佐证 | “酸低糖低=引流” |
| 食管癌吞咽困难 | 先液后固 | 典型为先固后液,进行性加重 | “硬的先卡住” |
| 食管癌分期工具 | CT即可判断T分期 | 内镜超声评估T分期最优;CT/PET评估转移 | “T看镜超,远看CT/PET” |
| 胸腺瘤诊疗 | 术前常规穿刺活检 | 多直接手术,不常规粗针活检以免播散 | “胸腺少穿刺” |
| 前纵隔鉴别 | 忘记4T | Thymoma/Thyroid/Teratoma/Terrible lymphoma | “前纵隔=4T” |
基础
甲状腺应用解剖
- 位置与被膜
- 甲状腺位于颈前区喉气管前外侧,由右、左叶与峡部组成,约50%有金字塔叶(锥状叶)。
- 外有颈深筋膜包绕形成“甲状腺外被膜”,贴腺体的纤维被膜为“甲状腺内被膜”,两者之间形成血管神经网。
- 与气管之间借Berry韧带紧密相连,行切除时须注意靠近气管环处的腺体残存可致复发。
- 邻近重要结构
- 上极:上甲状腺动脉与外侧喉上神经(上喉返支外侧支,支配环甲肌张力)关系密切,结扎上极血管时应在腺体近侧处理以保护外侧喉上神经。
- 后外侧:喉返神经走行于气管食管沟,入喉前常与下甲状腺动脉分支交叉,变异多;入喉点在环杓关节附近,为易损点。
- 后内侧:甲状旁腺多位于甲状腺后缘(上旁腺在上极后方、下旁腺在下极附近),其血供主要来自下甲状腺动脉分支。
- 血供
- 动脉:上甲状腺动脉(颈外动脉分支)、下甲状腺动脉(锁骨下动脉—甲状颈干分支),少数有甲状腺最下动脉(头臂干/主动脉弓分支)。
- 静脉:上、中、下甲状腺静脉丛,下甲状腺静脉汇入头臂静脉,术中出血多源于静脉丛撕裂。
- 淋巴引流
- 中央区(VI区):峡部与双侧叶内侧引流至预喉、喉前、气管前、气管旁淋巴结。
- 侧颈区(II–V区):外上象限多引流至颈深上组(II、III区)。
- 功能与手术要点
- 手术应保护:喉返神经、外侧喉上神经;尽量保留/自体移植甲状旁腺以预防低钙血症。
- 甲状腺包膜下切除可减少旁腺、喉返神经损伤风险。
| 结构 | 易损环节 | 保护要点/并发症要点 |
|---|---|---|
| 外侧喉上神经 | 上极血管处理 | 上极结扎靠腺体侧,分离时紧贴腺体,避免高位结扎致声调降低、高音唱不上去。 |
| 喉返神经 | 入喉点与Berry韧带 | 沿气管食管沟追踪,Berry韧带处锐性分离;损伤致声音嘶哑/呛咳,双侧损伤可致呼吸困难需气管切开。 |
| 甲状旁腺 | 下甲状腺动脉末支 | 保留腺体完整与血供,必要时自体移植(胸大肌/胸锁乳突肌);防低钙手足搐搦。 |
| 下甲状腺静脉丛 | 峡部/下极离断 | 术野清晰,逐支结扎;避免撕裂致术中大出血影响暴露与神经辨认。 |
弥漫性非毒性甲状腺肿(单纯性甲状腺肿)
病因
- 碘缺乏(最常见):山区/内陆缺碘地区,饮食碘摄入不足。
- 生理性:青春期、妊娠、哺乳期对甲状腺激素需求↑。
- 致甲状腺肿物质:某些食物(木薯、甘蓝)或药物(硫脲类、锂盐、胺碘酮)长期使用。
- 先天性甲状腺激素合成酶缺陷(少见)。
发病机制
- 碘缺乏或合成障碍 → T4/T3合成受限 → 垂体TSH代偿性升高 → 甲状腺滤泡上皮增生与胶质变化 → 弥漫肿大,可反复增生-退变致结节化。
临床表现
- 颈前对称性无痛性肿大,质地中等或稍韧,一般无压迫症状;甲状腺功能多正常(非毒性)。
- 长期巨大或胸骨后肿大可出现呼吸/吞咽受限、Pemberton征阳性(双臂上举颜面充血、呼吸困难)。
辅助检查
- 甲状腺功能:T3/T4多正常或轻低,TSH正常或轻高。
- 超声:弥漫性肿大,回声均匀或稍低;晚期可有结节。
- 放射性碘摄取率:碘缺乏者可弥漫性增高。
- 碘营养评估:尿碘降低。
诊断和鉴别诊断
- 依据地区、病史、体征与超声。
- 鉴别:Graves病(弥漫肿大伴甲亢与突眼)、慢性淋巴细胞性甲状腺炎(质地橡皮样、抗体阳性)、多结节性甲状腺肿(不规则结节)、亚急性甲状腺炎(疼痛+ESR高)。
| 疾病 | 核心线索 | 要点 |
|---|---|---|
| Graves病 | 弥漫肿+甲亢+突眼 | TRAb阳性;放射性碘摄取弥漫增高;血流丰富;抗甲状腺药/RAI/手术三选一。 |
| 亚急性甲状腺炎 | 疼痛+发热+ESR高 | 病毒后;游离T4↑、TSH↓,但放碘摄取显著降低;NSAIDs/激素+β阻滞,不需抗甲药。 |
| 慢性淋巴细胞性甲状腺炎 | 橡皮样肿大 | 抗TPO/抗TG高滴度;超声弥漫低回声;多为甲减期,左甲状腺素替代。 |
治疗
- 碘补充(首选):食盐加碘、碘化钾小剂量。
- 小剂量左甲状腺素抑制TSH(青年早期、短期应用;妊娠/老年/心血管病慎用)。
- 压迫或美容需求、胸骨后巨大肿/快速增大疑恶性:手术(腺叶+峡部切除或近全切)。
- 预防:全民食盐加碘。
甲状腺功能亢进的外科治疗
适应证
- 巨大甲状腺肿(尤其胸骨后/压迫症状)、复发性甲亢(抗甲状腺药失败/停药复发)、合并结节或癌变嫌疑、妊娠计划或抗甲药不耐受/禁忌、重度甲状腺相关眼病(RAI慎用),患者意愿。
术前准备(关键)
- 目标:达到甲状腺功能正常或近正常,以防甲危象。
- 抗甲状腺药(甲巯咪唑/丙硫氧嘧啶)+β受体阻滞剂控制心率。
- 手术前10–14天口服卢戈碘液或碘化钾,减少腺体血运。
- 必要时糖皮质激素(合并眼病或甲危象风险高)。
- 纠正贫血、电解质紊乱;合并感染/上呼吸道炎症需控制。
手术方式
- 双侧近全或全甲状腺切除:降低复发率(当前主流)。对巨大肿、复发、结节可疑肿瘤者优选。
- 选择性腺叶+峡部切除:病变侧明显、对侧轻度者可选,但复发风险较高。
- 伴显著淋巴结肿大/结节可行中央区清扫(非常规)。
术后并发症及处理
- 出血/呼吸道压迫:颈前血肿需紧急开口减压。
- 喉返神经损伤:声音嘶哑、误吸;双侧损伤致呼吸困难。
- 低钙血症/甲旁腺功能减退:口周手足麻木、抽搐,出现Trousseau/Chvostek征,静滴葡萄糖酸钙并补充钙剂+活性维生素D。
- 甲状腺危象预防:术前准备充分;术后观察体温、心率、精神状态。
与放射性碘/药物治疗选择
- 年轻、巨大甲状腺、孕期计划短期内、药物不耐受/复发 → 手术优先。
- 老年/合并症多/腺体不大 → RAI考虑。
- 轻中度初发 → 抗甲状腺药起始;复发再评估。
亚急性甲状腺炎(De Quervain)
病因
- 多在上呼吸道病毒感染后,肉芽肿性炎。
发病机制
- 滤泡破坏→预存激素逸出→一过性甲亢期,随后进入低功能期,最终多恢复。
临床表现
- 颈前甲状腺疼痛(可放射至下颌/耳),压痛明显;发热、乏力。
- 甲亢样症状(心悸、出汗)多为一过性。
辅助检查
- ESR/CRP明显升高;FT4/FT3↑、TSH↓。
- 放射性碘摄取率显著降低。
- 超声低回声片灶+血流减少;抗体阴性或低滴度。
诊断和鉴别诊断
- 疼痛+ESR高+摄取率低基本确诊。
- 鉴别:Graves(摄取高、突眼)、化脓性甲状腺炎(高热、白细胞高、脓肿形成)、桥本(慢性无痛)。
治疗
- 轻中度:NSAIDs。
- 重度疼痛或发热:泼尼松20–40 mg起,2–4周缓停。
- β受体阻滞剂对症;不推荐抗甲状腺药。
- 低功能期短期左甲状腺素替代。
慢性淋巴细胞性甲状腺炎(桥本甲状腺炎)
病因
- 自身免疫性疾病,遗传易感与环境因素相关;常与其他自身免疫病并存。
发病机制
- 抗体(抗TPO、抗TG)介导的淋巴细胞浸润与滤泡破坏 → 逐渐甲减。
临床表现
- 颈前橡皮样弥漫肿大,进展缓慢;早期可短暂甲亢(破坏性释放),多随后转甲减。
辅助检查
- 抗TPO/抗TG高滴度阳性。
- 超声弥漫低回声、粗糙、血流减少。
- FNA:淋巴细胞浸润、Hürthle细胞化生。
诊断和鉴别诊断
- 抗体阳性+超声特征。
- 警惕并发甲状腺淋巴瘤(腺体迅速增大、压迫明显)。
治疗
- 左甲状腺素替代(TSH为靶);妊娠期TSH目标更严格。
- 肿大压迫/怀疑肿瘤:手术活检/切除。
- 随访TSH与腺体体积。
甲状腺癌
病因
- 放射暴露、家族史(RET突变导致髓样癌/MEN2)、甲状腺结节长期存在等。
发病机制与类型
- 乳头状癌(最常见,淋巴转移倾向)
- 滤泡癌(血行转移至骨/肺)
- 髓样癌(C细胞来源,降钙素与CEA升高)
- 未分化癌(进展最快,预后差)
| 类型 | 转移/标志物 | 治疗要点 |
|---|---|---|
| 乳头状癌 | 淋巴结转移常见 | 优选腺叶+峡部或全切;中高危配合131I与TSH抑制。 |
| 滤泡癌 | 血行转移(骨/肺) | 多行全切+131I;需要病理证实包膜/血管侵犯。 |
| 髓样癌 | 降钙素、CEA↑;RET相关 | 全切+中央区清扫;不行131I;随访以降钙素为主。 |
| 未分化癌 | 极快进展 | 以气道管理+放/化疗/靶向为主,预后差。 |
临床表现
- 颈部无痛性结节,质硬不均、边界不清、固定;颈淋巴结肿大;声音嘶哑、吞咽困难提示侵犯。
辅助检查
- 超声:TI-RADS评估,恶性征象如微钙化、纵横比>1、边界不清、形态不规则。
- FNA细针穿刺细胞学:Bethesda分级。
- 实验室:降钙素(髓样癌)、甲状腺球蛋白(分化型术后随访)。
- 影像:颈部超声分区淋巴结评估;CT/MRI评估侵犯;分化型术后随访可用131I全身显像。
诊断和鉴别诊断
- FNA为诊断核心;滤泡性病变需病理证实包膜/血管侵犯方可定性。
治疗
- 手术
- 全甲状腺切除:多灶/>1 cm伴不良因素、对侧病灶、放射史、远处转移、髓样癌/未分化癌。
- 腺叶+峡部切除:低危单灶乳头状微癌(≤1 cm)、无高危因素者可选。
- 淋巴结清扫:临床阳性N1行治疗性清扫;部分高危分化癌可考虑中央区预防性清扫。
- 131I治疗:中高危分化型术后残灶/微转移清除与复发监测。
- TSH抑制:左甲状腺素抑制治疗(中高危更严格)。
- 髓样癌:全切+中央区清扫,监测降钙素;RET检测与家系筛查。
- 未分化癌:以姑息/综合治疗为主(气道保障、放化疗/靶向)。
- 靶向/免疫:难治性分化癌或晚期髓样癌可用多靶点TKI等。
甲状旁腺功能亢进症
病因
- 原发性(最常见为单发腺瘤),也见于腺体增生/癌。
- 继发性:慢性肾衰、维生素D缺乏致长期低钙刺激。
- 三发性:长期继发性基础上旁腺自律性增生(肾移植后常见)。
发病机制
- PTH过多→骨吸收↑、肾小管钙重吸收↑、磷排泄↑、肠钙吸收↑(维生素D活化)。
临床表现
- “骨痛、肾结石、胃肠不适、精神症状”:骨质疏松/病理骨折;肾结石/肾钙化;乏力、抑郁、便秘、多尿、多饮。
- 体检:股骨颈/椎体压痛,肌无力。
辅助检查
- 实验室:血钙↑、血磷↓、PTH↑(原发);继发性多为钙低或正常、PTH↑。
- 影像定位:颈部超声、99mTc-MIBI显像(首选定位)、CT/MRI。
- 骨代谢:骨密度降低;尿钙↑(除FHH)。
诊断和鉴别诊断
- 鉴别家族性低尿钙性高钙血症(FHH,尿钙低)。
- 结合肾功能判断继发/三发性。
治疗
- 原发性:甲状旁腺切除(腺瘤切除或3.5腺切除用于增生);术中快速PTH监测评估切除充分。
- 继发性:限制磷、活性维生素D、钙拟似物;难治者旁腺切除。
- 高钙危象:补液+袢利尿、降钙药(降钙素、双膦酸盐)、必要时血液透析。
急性乳腺炎
病因
- 多发生于哺乳期(产后2–6周);主要致病菌为金黄色葡萄球菌,经乳头裂隙进入。
发病机制
- 导管阻塞/乳汁潴留→细菌繁殖→急性炎症,晚期可形成乳腺脓肿。
临床表现
- 局部红、肿、热、痛,条索样硬结;发热、寒战;挤压疼痛明显。
- 脓肿形成时波动感、疼痛加重。
辅助检查
- 超声有助判断脓肿腔;血常规白细胞↑、CRP↑。
诊断和鉴别诊断
- 基于哺乳史+急性局部炎症;鉴别炎性乳腺癌(进展快、皮肤橘皮样、腋结大)。
治疗
- 继续排空乳汁(哺乳/吸乳器),热敷按摩通畅导管。
- 抗菌药物:对葡萄球菌有效(青霉素酶稳定青霉素/头孢/克林霉素;MRSA地区按指引)。
- 形成脓肿:切开引流(乳晕放射状切口)或超声引导穿刺置管;培养选药。
- 对症:止痛退热;纠正脱水与营养。
乳腺囊性增生病(纤维囊性病变)
病因
- 雌孕激素比例失衡与周期性乳腺反应相关。
发病机制
- 小叶腺泡与导管囊性扩张,伴纤维化与腺上皮增生。
临床表现
- 青壮年女性,周期性乳胀与胀痛;双侧、弥漫或多发结节,边界尚清,随月经波动。
辅助检查
- 乳腺超声:多发小囊肿、纤维化回声;必要时钼靶。
- 可穿刺抽吸:抽出清亮/草黄色液体,肿块缩小消失。
诊断和鉴别诊断
- 与乳腺癌鉴别:癌多质硬不规则、固定、无周期性疼痛,必要时穿刺/活检。
| 疾病 | 典型体征 | 影像/处理要点 |
|---|---|---|
| 纤维腺瘤 | 可推动、界清、质中等,年轻女性 | 超声椭圆等/低回声,随访或切除(>3 cm/生长快)。 |
| 囊性增生 | 周期性胀痛、多发小结节 | 超声多发小囊;穿刺抽吸液体消退;对症治疗。 |
| 导管内乳头状瘤 | 单孔血性溢乳 | 导管影像/超声提示;微乳管切除。 |
| 乳腺癌 | 质硬、不规则、固定;皮肤橘皮、酒窝征 | 粗针活检确诊;手术+系统治疗+放疗综合管理。 |
治疗
- 生活方式:减少咖啡/巧克力,佩戴合适胸罩。
- 对症:非甾体镇痛;局部/短程药物(如孕激素、达那唑)个体化。
- 可疑结节或反复回抽出血性液体:手术切除病灶。
乳房纤维腺瘤
病因与发病机制
- 雌激素相关的纤维与腺体成分比例异常增生,年轻女性最常见良性肿瘤。
临床表现
- 单发为主,质中等、界清、可推动(“乳房滑动瘤”),随月经轻度变化。
辅助检查
- 超声:椭圆形、边界清、后方回声增强。
- 三联评估(查体+影像+细针/粗针):大多可明确。
诊断和鉴别诊断
- 与叶状肿瘤(生长较快、可巨大)及癌(不规则、浸润)鉴别。
治疗
- 小而稳定者可随访;>3 cm、快速生长、可疑影像学特征或患者焦虑:手术切除(保留美容)。
乳房导管内乳头状瘤
病因与发病机制
- 导管内上皮乳头状增生形成肿物,多位于乳晕后大导管。
临床表现
- 单孔血性溢乳最典型;常触不到肿块或可触及乳晕后小结节。
辅助检查
- 超声/导管成像(必要时乳管镜);分泌物细胞学。
诊断和鉴别诊断
- 鉴别乳腺癌(尤其导管内癌)与乳头湿疹/乳头溢液综合征。
治疗
- 微乳管切除(微导管切除)为首选;病理证实伴不典型增生或癌变时按癌处理。
乳房肉瘤
病因与类型
- 罕见,来源于乳腺间质(纤维肉瘤、血管肉瘤等);与放疗史相关的继发性血管肉瘤需警惕。
- 叶状肿瘤虽为纤维上皮性肿瘤,但高分级/恶性叶状肿瘤生物学类似肉瘤。
临床表现
- 生长较快、较大、界相对清,但可侵袭;皮肤紧张变薄、溃破。
辅助检查
- 影像难以与良恶性区分;粗针活检或切除活检确诊。
治疗
- 广泛局部切除或改良根治性切除,确保足够切缘;常规腋窝清扫不必需(淋巴转移少见)。
- 放/化疗根据分级、大小、切缘决定;血管肉瘤对化疗较敏感。
乳腺癌
病因与高危因素
- 年龄、月经初潮早/绝经晚、未育或初产晚、家族/遗传(BRCA1/2)、雌激素暴露长、放射暴露、肥胖等。
发病机制
- 多源于导管上皮(导管癌),分子分型(Luminal A/B、HER2阳性、三阴性)决定系统治疗。
临床表现
- 无痛性肿块,质硬、界不清、固定,压痛少见;皮肤凹陷、酒窝征、橘皮样、乳头回缩、溢液;腋窝淋巴结肿大。
| 临床表现 | 特征描述 |
|---|---|
| 单发肿块 | 患侧乳房无痛、单发的肿块,质硬,表面不光滑,与周围组织分界不清,活动度差 |
| 乳头溢液 | 5%~10%的病人首发症状是乳头血性溢液 |
| 酒窝征 | 癌肿累及Cooper韧带,使其缩短而致肿瘤表面皮肤凹陷 |
| 乳头凹陷 | 邻近乳头、乳晕时侵入乳管使之缩短,可把乳头牵向一侧引起乳头凹陷 |
| "橘皮样"改变 | 癌细胞堵塞皮下淋巴管,引起淋巴回流障碍,出现真皮水肿,皮肤呈现"橘皮样"改变 |
| 卫星结节 | 癌细胞沿皮下淋巴网广泛扩散到乳房及其周围皮肤,形成小结节 |
| 手臂白色水肿 | 癌细胞堵塞腋窝主要的淋巴管,引起该侧手臂淋巴回流障碍,发生的蜡白色手臂水肿 |
| 手臂青紫水肿 | 锁骨下或腋窝变硬的淋巴结压迫腋静脉,引起的该侧手臂青紫色水肿 |
| 炎性乳腺癌 | 少见,发展迅速,预后差。局部皮肤可呈炎症样表现,发红、水肿、增厚、粗糙、表面温度升高,偶有疼痛。治疗采用放化疗,禁忌手术 |
| Paget病 | 即乳头湿疹样乳腺癌。少见,恶性程度低,发展慢,乳头有瘙痒、烧灼感,以后出现乳头和乳晕的皮肤变粗糙、糜烂如湿疹样,进而形成溃疡,局部反复出现结痂和脱屑 |
辅助检查
- 影像:钼靶+超声;必要时MRI。
- 病理:粗针活检为首选;免疫表型ER/PR、HER2、Ki-67。
- 分期:TNM;全身评估(骨/胸/腹)。
诊断和鉴别诊断
- 三联评估一致性高;疑难者手术切除病检。
- ✨临床分期:N分期不是看淋巴结数量,而是看淋巴结与周围组织的关系
| 临床分期 | 对应 TNM | 要点 |
|---|---|---|
| 0 期 | Tis N0 M0 | 原位癌;无淋巴结转移、无远处转移。 |
| I 期 | T1 N0 M0 | 肿瘤≤2 cm、无区域淋巴结转移,局限性手术可治愈率高。 |
| II 期 | T0–T2 N0–N1 M0 (常分 IIA / IIB) | T1–T2(≤5 cm)或同侧可触及淋巴结: - IIA:T0–T1 N1 M0 或 T2 N0 M0 - IIB:T2 N1 M0 或 T3 N0 M0(T3>5 cm) |
| III 期 | 局部晚期,T0–T4 N2–N3 M0(细分 IIIA/IIIB/IIIC) | 局部侵犯或广泛区域淋巴结受累、但无远处转移: - IIIA:T0–2 N2 M0 或 T3 N1–2 M0 - IIIB:T4(任何 N)M0(侵及胸壁/皮肤/炎性乳癌) - IIIC:任何 T N3 M0(锁骨上/锁骨下/固定淋巴结) |
| IV 期 | 任何 T、任何 N、M1 | 有远处转移(骨、肺、肝、脑等),以系统治疗为主,治愈性较低。 |
| TNM 关键定义 | T:Tis(原位);T1≤2 cm;T2>2–≤5 cm;T3>5 cm;T4侵犯胸壁或皮肤(含炎性乳癌)。 N:N0 无淋巴结转移;N1 可推动同侧腋窝淋巴结肿大;N2 固定或融合/内乳淋巴结受累;N3 锁骨上/锁骨下或广泛淋巴结受累。 M:M0 无远处转移;M1 有远处转移。 | |
治疗
①I、II期乳腺癌原首选 Halsted 手术,现首选乳腺癌改良根治术。
②位于内象限的乳腺癌,若有胸骨旁淋巴结转移,首选乳腺癌扩大根治术(Urban 手术)。
③乳腺原位癌、微小癌,可选择全乳房切除术,术后补充放疗。
④保留乳房的乳腺癌切除术术后必须辅以放疗。
- 基本路径
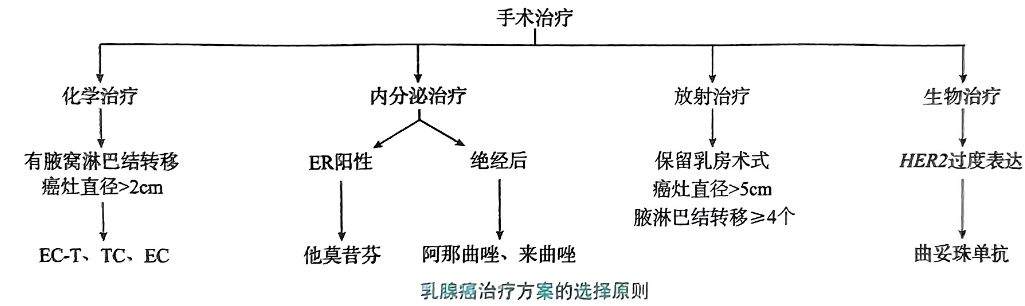
- 局部手术
- 保乳+前哨淋巴结活检(SLNB)适用于早期;切缘阴性+术后放疗。
- 不能保乳或患者意愿:改良根治(乳腺切除+腋窝处理)。
- 腋窝:cN0行SLNB;阳性(宏转移)多需ALND或区域照射。
| 手术名称 | 手术方式 | 适应证 |
|---|---|---|
| 乳腺癌根治术(Halsted 手术) | 切除整个乳房、胸大肌、胸小肌及Ⅰ、Ⅱ、Ⅲ组腋窝淋巴结的整块切除。 | 适用于肿瘤侵及胸大肌和胸小肌者。为过去乳腺癌标准根治术,现已少用。 |
| 乳腺癌扩大根治术(Urban 手术) | 在 Halsted 基础上加胸廓内动、静脉及其周围淋巴结(即胸骨旁淋巴结)切除。 | 适用于肿瘤侵及胸骨旁淋巴结者,手术范围大,现较少使用。 |
| 乳腺癌改良根治术(Patey 手术) | 保留胸大肌或胸小肌(与传统 Halsted 相比),切除乳房及腋窝淋巴结,保留胸肌,术后外观较好。 | 适用于Ⅰ、Ⅱ期乳腺癌,目前常用的根治方式。 |
| 全乳房切除术 | 切除整个乳房,含腋尾部及胸大肌筋膜(不切肌肉本身)。 | 局部广泛病变、微小癌、或体质较弱/高龄患者不宜保乳时采用。 |
| 保留乳房的乳腺癌切除术(乳房保留术) | 切除肿瘤及周围1–2cm正常组织,确保标本边缘无肿瘤细胞。 | 适用于Ⅰ、Ⅱ期乳腺癌,术后需辅以放疗;外观效果好,近年来在我国逐步增多。 |
| 前哨淋巴结活检术 + 腋淋巴结清扫术 | 对临床淋巴结阴性者先行前哨淋巴结活检;若病理阳性再行腋淋巴结清扫;前哨结为乳腺肿瘤淋巴引流的第一站,可用蓝染或放射示踪定位并活检。 | 临床腋淋巴结阴性者可先做前哨活检;病理决定是否行清扫。前哨阴性者可避免常规腋清扫。 |
| 乳腺腔镜手术 | 经小切口或皮下隧道行部分或全部乳房切除,配合腋窝淋巴结检査/清扫、乳房重建或假体植入等。 | 适用于切口隐蔽、创伤小且对美容有要求的患者;须根据肿瘤大小、位置及淋巴结情况慎重选择。 |
- 全身治疗
- 内分泌治疗:ER/PR阳性(绝经前他莫昔芬±卵巢抑制;绝经后芳香化酶抑制剂)。
- 抗HER2治疗:曲妥珠单抗±帕妥珠单抗。
- 化疗:三阴性或高危。基本上以
环磷酰胺为基础。差用EC-T,好用TC/EC。 - 新辅助治疗:降期以利保乳/手术。
| 治疗类型 | 分类 | 具体内容 |
|---|---|---|
| 化学治疗 | 特点 | 乳腺癌是实体瘤中化疗最有效的肿瘤之一,化疗在整个治疗中占有重要地位 |
| 术后辅助化疗指征 | ①浸润性乳腺癌伴腋淋巴结转移;②腋淋巴结阴性而有高危复发因素者:原发肿瘤直径>2cm,组织学分级差,雌、孕激素受体阴性,癌基因HER2有过度表达 | |
| 化疗方案 | 肿瘤分化差、分期晚:EC-T方案(表柔比星+环磷酰胺+多西他赛或紫杉醇) 肿瘤分化较好、分期较早:TC方案(多西他赛或紫杉醇+环磷酰胺)、EC方案(表柔比星+环磷酰胺) | |
| 术前化疗 | 多用于肿瘤较大的三阴性和HER2阳性的病例,目的在于缩小肿瘤和/或区域淋巴结转移的大小,提高手术成功率 | |
| 内分泌治疗 | 适应症 | ER和PR阳性者,约占所有乳腺癌病人的70%,称激素依赖性肿瘤。ER阴性者称激素非依赖性肿瘤,对抗雌激素治疗反应差 |
| 他莫昔芬 | 最常用的抗雌激素类药物,通过与雌激素受体竞争结合,阻断雌激素进入肿瘤细胞,抑制其生长,减少术后复发及转移 | |
| 芳香化酶抑制剂 | 阿那曲唑、来曲唑、依西美坦,对绝经后病人效果优于他莫昔芬,能抑制肾上腺分泌的雄激素转变为雌激素过程中的芳香化环节,从而降低雌二醇 | |
| 放射治疗 | 适应症 | ①保留乳房的乳腺癌手术后,放射治疗是重要组成部分;②乳房切除术后:原发肿瘤直径≥5cm,或腋淋巴结转移≥4个,或1~3个淋巴结转移伴有高危因素者 |
| 靶向治疗 | 适应症与药物 | 对于表皮生长因子受体(HER2)基因过度表达的乳腺癌,可使用曲妥珠单抗治疗 |
- 放疗:保乳术后常规;高危切除后。
- 特殊:炎性乳腺癌首选新辅助化疗→手术→放疗。
- 随访:体检+影像;骨/内脏转移个体化治疗。
肋骨骨折
病因
- 钝性胸部外伤最常见;多发骨折可致连枷胸。
发病机制
- 骨折端活动致疼痛、浅表呼吸;多发双处骨折形成胸壁反常呼吸。
临床表现
- 局部压痛、叩痛、呼吸运动痛,可触及骨擦音;连枷胸见反常呼吸。
- 合并伤:气胸、血胸、肺挫伤。
辅助检查
- 胸片/CT明确骨折与并发症;血气评估通气。
诊断和鉴别诊断
- 体征+影像;警惕老年患者并发呼吸衰竭。
治疗
- 镇痛(口服/静脉、肋间神经阻滞、PCA)、呼吸功能锻炼、咳痰。
- 合并气/血胸:胸腔闭式引流。
- 连枷胸/重度通气障碍:机械通气、必要时外固定/内固定。
气胸
病因
- 自发性(原发:肺大疱破裂;继发:COPD、结核等);医源性/外伤性。
发病机制
- 胸膜破裂→气体进入胸膜腔→肺萎陷;张力性气胸形成单向活瓣致纵隔移位、休克。
临床表现
- 突发胸痛、呼吸困难;体检:患侧过清音、呼吸音减弱/消失;张力性气胸静脉怒张、低血压、气管偏移。
辅助检查
- 胸片:肺萎陷线;立位吸气更敏感;CT更敏感。
- 超声:滑动征消失、肺点。
诊断和鉴别诊断
- 临床+影像;张力性以临床为先导,不等影像先行减压。
| 情况 | 体征/检查 | 首要处理 |
|---|---|---|
| 气胸 | 过清音、呼吸音减弱;胸片肺缘线 | 胸管引流;张力性先针刺减压后胸管。 |
| 血胸 | 浊音、致密影;休克征 | 粗胸管引流+复苏;大量血胸指征开胸止血。 |
| 脓胸 | 脓性胸液,pH<7.2、糖低、LDH高 | 抗生素+充分引流;必要时纤溶/VATS剥脱。 |
治疗
- 小量稳定:氧疗+观察。
- 有症状/较大:胸腔闭式引流(第4–5肋间前腋线)。
- 张力性:立即针刺减压(传统第2肋间锁骨中线,或更推荐第4–5肋间腋前/中线)→胸管。
- 复发/持续漏气/双侧/职业高风险:VATS切除肺大疱+胸膜固定。
血胸
病因
- 胸部外伤(肋间血管、肺裂伤、内乳/大血管);术后并发症。
发病机制
- 血液进入胸膜腔,压迫肺致通气障碍与失血性休克。
临床表现
- 呼吸困难、面色苍白、叩诊浊音、呼吸音减弱;循环不稳。
辅助检查
- 胸片:液气平面/致密阴影;超声敏感;CT定位出血源。
- 血红蛋白下降、休克指标。
诊断和鉴别诊断
- 与大量胸腔积液、恶性胸水鉴别;结合创伤史。
治疗
- 胸腔闭式引流(较粗胸管);补液/输血纠正休克。
- 大量血胸指征行急诊开胸止血:初次引流>1500 mL或持续出血>200 mL/h(持续2–4 h)、合并血流动力学不稳、疑及大血管/心脏/膈损伤。
脓胸(化脓性胸膜炎)
病因
- 肺炎旁胸腔积液进展、胸外伤/术后、食管穿孔等。
发病机制
- 三期:渗出期→纤维脓性期→机化期(纤维包裹肺不张)。
临床表现
- 发热、胸痛、呼吸困难;体征与胸腔积液相似。
辅助检查
- 胸腔穿刺液化验:脓性、pH<7.2、葡萄糖<2.2 mmol/L、LDH高、细菌阳性。
- 影像:超声分隔、CT显示包裹征。
诊断和鉴别诊断
- 依据感染证据+胸液特征;与结核性胸膜炎/恶性胸水鉴别。
治疗
- 抗生素;胸腔引流充分。
- 隔腔/黏连:纤溶剂(tPA/DNase)腔内注入。
- 机化期或引流失败:VATS清创剥脱或开胸剥脱。
食管癌
病因
- 我国以鳞癌多见;危险因素:吸烟、饮酒、热烫/腌制食物、营养缺乏、食管上皮不典型增生;腺癌与Barrett食管/胃食管反流相关。
发病机制
- 上皮异型增生→原位癌→浸润癌;淋巴管丰富,跳跃式转移常见。
临床表现
- 进行性吞咽困难(先固后液)、胸骨后不适/疼痛、体重下降;晚期呛咳(食管气道瘘)、声音嘶哑。
| 部位 | 常见病理 | 术式要点 |
|---|---|---|
| 颈段/上胸段 | 鳞癌多见 | McKeown三切口食管切除+颈胸腹淋巴清扫,胃代食管/结肠代食管。 |
| 中胸段 | 鳞癌最多 | Ivor-Lewis(胸腹两切口)或McKeown,吻合位胸内/颈部。 |
| 下胸段/贲门 | 腺癌相对多 | Ivor-Lewis/经膈肌入路,必要时与胃底联合处理。 |
辅助检查
- 电子内镜+活检(确诊);内镜超声评估T分期与局部结节。
- 影像:增强CT胸腹、必要时PET-CT评估远处转移。
- 营养评估。
诊断和鉴别诊断
- 与良性狭窄(腐蚀/瘢痕)、贲门失弛缓鉴别。
治疗
- 早期(T1a):内镜下黏膜/黏膜下剥离(EMR/ESD)±局部消融。
- 可切除局限期:食管切除重建(Ivor-Lewis、McKeown等)+系统淋巴结清扫;新辅助放化疗可降期提高R0率。
- 局部晚期不宜手术或不愿手术:根治性放化疗(鳞癌敏感)。
- 姑息:支架、营养通道、止痛、免疫/靶向个体化。
纵隔肿瘤
病因与分区
- 前纵隔:4T(胸腺瘤Thymoma、甲状腺异位/甲状舌管囊肿Thyroid、畸胎瘤/生殖细胞瘤Teratoma、淋巴瘤Terrible lymphoma)。
- 中纵隔:支气管源性囊肿、心包囊肿、淋巴结肿大。
- 后纵隔:神经源性肿瘤(神经鞘瘤、神经节瘤)最常见。
发病机制
- 多为局部占位压迫,引起气管、食管、上腔静脉/神经症状;胸腺瘤可合并重症肌无力。
临床表现
- 咳嗽、气促、吞咽困难、胸痛、上腔静脉综合征;部分无症状体检发现。
| 分区 | 高发肿瘤 | 诊断/治疗要点 |
|---|---|---|
| 前纵隔 | 4T:胸腺瘤、甲状腺、畸胎瘤、淋巴瘤 | 查AFP/β-hCG;胸腺瘤合并肌无力;多以手术为主,淋巴瘤化疗。 |
| 中纵隔 | 支气管囊肿、心包囊肿、淋巴结 | CT示薄壁囊性;症状明显或感染复发时切除。 |
| 后纵隔 | 神经源性肿瘤 | MRI评估椎管受累;外科切除效果好。 |
辅助检查
- 增强CT(首选分区与关系评估)、MRI(神经源性/心包病变)、肿瘤标志物:AFP、β-hCG(生殖细胞瘤),降钙素/甲功(异位甲状腺)。
- 必要时经皮粗针活检(疑淋巴瘤等);胸腺瘤多直接手术,不常规活检以免播散。
诊断和鉴别诊断
- 依据分区+影像特征+肿瘤标志物;鉴别血管性病变(需血管成像)。
治疗
- 手术切除为主(胸腺瘤全胸腺切除);生殖细胞瘤视类型行化疗/放疗(精原细胞瘤对放疗敏感、非精原细胞瘤对化疗敏感)。
- 淋巴瘤以化疗±放疗为主。